Por: Luana Probst, Letícia Cardoso e Morgana de Souza
Eletroquimioterapia como Tratamento para Carcinoma Espinocelular em Felino: Relato de Caso
Electrochemotherapy as a treatment for feline spinocellular carcinoma: a case report
RESUMO
O carcinoma de células escamosas (CCE), carcinoma espinocelular (CEC), carcinoma escamocelular ou carcinoma epidermóide, é uma neoplasia maligna cutânea que aparece comumente nos felinos, apresentando nesta espécie um comportamento distinto das demais espécies. Há dois fatores etiológicos que podem explicar o aparecimento desta patologia, a exposição prolongada à luz ultravioleta (UV), assim como as áreas hipopigmentadas e com poucos pelos, que são as mais afetadas. Sabe-se que os gatos de pelagem branca são mais predispostos a apresentar a doença quando comparado aos pigmentados. Quanto a localização, a maioria das lesões são observadas na região da cabeça e mais frequentemente no plano nasal, seguida pelas aurículas e pálpebras, e podem se apresentar de formas variadas como proliferativa ou erosiva. O diagnóstico sugestivo vem através do histórico do paciente e das apresentações clínicas das lesões, para o diagnóstico definitivo é necessário realizar exame citológico. Existem várias formas de tratamento para o CEC, como cirurgia, radiação ionizante, quimioterapia, terapia fotodinâmica, eletroquimioterapia e criocirurgia. O objetivo deste trabalho foi relatar o caso de um felino diagnosticado com carcinoma de células escamosas tratados com a técnica de eletroquimioterapia e sua efetividade.
{PAYWALL_INICIO}
Palavras-chave: CEC, felino, eletroquimioterapia, carcinoma.
ABSTRACT
Squamous cell carcinoma (SCC) or epidermoid carcinoma, is a malignant cutaneous neoplasm that appears commonly in cats, presenting in this species a distinct behavior from other species. There are two etiological factors that may explain the appearance of this pathology, prolonged exposure to ultraviolet light (UV), as well as hypopigmented areas with little hair, which are the most affected. It is known that white-coated cats are more predisposed to the disease when compared to pigmented cats. As for the location, most lesions are observed in the head region and most often in the nasal plane, followed by the auricles and eyelids, and may present in various forms such as proliferative or erosive. The suggestive diagnosis comes through the patient’s history and the clinical presentations of the lesions, for the definitive diagnosis it is necessary to perform a cytological examination. There are several forms of treatment for SCC, such as surgery, ionizing radiation, chemotherapy, photodynamic therapy, electrochemotherapy and cryosurgery. The objective of this paper was to report the case of a feline diagnosed with squamous cell carcinoma treated with the technique of electrochemotherapy and its effectiveness.
Palavras-chave: SCC, feline, electrochemoteraphy, carcinoma.
INTRODUÇÃO
Em 1998, a Organização Mundial da Saúde (OMS) deu uma nova classificação histológica detalhada aos tumores de pele epiteliais e mesenquimais em animais domésticos.1 Os tumores cutâneos foram então classificados pelo tipo de tecido envolvido, sendo: epitelial, estruturas anexas à pele, mesenquimal, células redondas ou melanócitos.2,6 Segundo estes autores, os tumores epiteliais compreendem tumores de células basais, papilomas, tumores subungueais e CCE.
Em gatos, os quatro tumores de pele com maior prevalência (compreendendo 70% dos casos de tumores de pele em felinos) são os de células basais, mastocitomas, CCEs e fibrossarcomas.3 Um estudo retrospectivo para avaliar a casuística de tumores em gatos na Cidade do México, utilizando 685 casos, concluiu que os tumores epiteliais foram os mais encontrados (56% dos casos), sendo o CCE o mais comum (117 casos).4
O CCE é uma neoplasia maligna diagnosticada comumente em cães e gatos, que gera uma diferenciação entre os queratinócitos, sendo a causa mais comum a alta exposição aos raios UV oriundos do sol.2 A falta de pigmentação da epiderme e a falta de pelos ou rarefação pilosa também são fatores coadjuvantes.1
Primeiramente, é importante entender que existem alguns tipos de tumores de queratinócitos, e que eles geram diferenciações entre essas células. O carcinoma de células escamosas multicêntrico in situ, ou carcinoma bowenoide in situ (BISC) é causado por infecções por papilomavírus, e pode ter fatores agravantes imunossupressores, como infecções por FIV e FeLV, ou tratamento com prednisolona e ciclosporinas, por exemplo.2 Já o CCE está altamente interligado com a alta exposição aos raios UV provindos do sol, juntamente com áreas geográficas que propiciam maior incidência solar. A falta de pigmentação da epiderme e a falta de pelos ou rarefação pilosa também são fatores coadjuvantes.1 Um estudo contendo felinos infectados com o vírus da FIV demonstrou que 24% desses gatos desenvolveram CCE, mas não está clara a relação exata com a doença e se teve algum fator externo (como exposição solar).5
Ainda assim, a anomalia genética responsável pelo desenvolvimento dessa neoplasia não foi muito bem elucidada, embora alguns estudos venham correlacionando com uma mutação que ocorre na proteína p53.3 Essa proteína é responsável por codificar uma fosfoproteína de 393 aminoácidos auxiliadora na etapa de transcrição do DNA, e sua produção é aumentada conforme a exposição à luz UV, a radiações ionizantes e a fármacos radiomiméticos; conforme ocorrem mutações e superexpressões da p53, o processo de carcinogênese pode ser iniciado.2
A maior prevalência de CCE está em cães idosos (entre 6 e 10 anos), de pelagem curta branca ou mesclada, sem predisposição sexual, das raças Keeshond, Schnauzer, Basset Hound, Border Collie, Dálmata, Pitbull Terrier e Beagle, e gatos de pelagens brancas, ou pelos faciais brancos, com idade entre 9 e 14 anos, sem predisposição racial ou sexual.2 Gatos siameses, himalaios e persas aparentam ter um risco reduzido em desenvolver essa neoplasia.3 Gatos de pelo branco têm 13,4 vezes o risco de desenvolver CCE de cabeça e pescoço em comparação com gatos de pelagem de cor mais escura.6
A incidência do CEC depende do tempo de exposição ao sol dos cães e gatos predispostos. Os gatos têm predisposição em desenvolver este tumor na região da cabeça, particularmente nas regiões com menor quantidade de pelos, geralmente em plano nasal ou pavilhão auricular e região circundante.3 Também pode ser visto na região do pescoço, nas pálpebras e áreas pré-auriculares.6 Em cães, é mais visto nas pálpebras, no plano nasal, no abdome, no tórax ventral e na parte medial dos membros pélvicos.2
As lesões podem se desenvolver em placas ou em formato papilar, com aspecto fungiforme ou crateriforme, e ainda podem ser eritematosas, ulceradas ou crostosas, apresentando hemorragia ou não.3 Metástases acontecem com pouca frequência, sendo mais comuns as regionais, como na pele e em linfonodos adjacentes, e incomuns as distantes, seja para linfonodos mais distantes, ou órgãos, como os pulmões.2
Para definição diagnóstica, além de uma anamnese criteriosa e um exame físico detalhado, se faz necessário estudo citológico e histopatológico, visto que há diversas formas de apresentação dos carcinomas de células escamosas.7 O tumor tem graus variados de diferenciação, sendo possível encontrar citologicamente, em um mesmo tumor, células basilares, células queratinizadas maduras, ou ambas.3 Os autores afirmam que para diferenciar o CEC de uma lesão inflamatória primária com epitélio escamoso displásico é necessário avaliar o grau de pleomorfismo (anisocitose e anisocariose moderada a acentuada, hipercromasia e atipia nuclear acentuada), a localização e aparência da lesão, e não deixar de realizar um exame histopatológico. A tomografia pode ser uma boa alternativa nos casos em que há massas de grades extensões, aderidas e infiltrativas.7
O passo a passo diagnóstico normalmente se baseia em: citologia por Punção Aspirativa por Agulha Fina (PAAF) como triagem, histopatologia e imuno-histoquímica, sendo que esta última utiliza principalmente dos seguintes marcadores: AE1/AE3, CK5/6, CK8, CK13, S-¬100, CAM 5.2 (CK7/8), a-¬SMA, MITF¬-M e Vimentina.2 Quando se trata do CCE, o estadiamento é feito com base nos métodos de diagnóstico citados e no sistema TNM (Tumor size, Lymph Nodes and Metastasis), avaliando se o tumor é massivo, com acometimento em linfonodos e potencial metastático.2 Os testes de estadiamento clínico adicionais são indicados para a formação de um plano de tratamento adequado e fornecem uma expectativa realista de prognóstico; incluem uma avaliação dos linfonodos regionais, radiografias torácicas com 3 projeções e ultrassonografia.6
Para o CCE, a prevenção pode ser feita principalmente em pacientes que se enquadram no grupo de prevalência, ou que possuem ceratose actínica (que pode evoluir para a neoplasia aqui citada), utilizando de medidas que não permitam exposição solar desprotegida, como roupas e filtro solar a cada 4 horas nas regiões com menor quantidade de pelos.2
Diversas são as opções para tentar alcançar o controle tumoral local em pacientes veterinários, todavia as terapias adjuvantes mais notáveis no espectro da oncologia veterinária são a quimioterapia, a remoção parcial ou total cirúrgica, a imunoterapia, a crioterapia, a radioterapia e a eletroquimioterapia (EQT).3,8 Esses tratamentos são mais eficazes quando as lesões são pequenas (menores que 5 cm) e superficiais, portanto, o diagnóstico precoce e a terapia imediata são essenciais.5
O controle da inflamação epidérmica pode ser feito com anti-inflamatórios não esteroidais (como firocoxibe 5 mg/kg, VO, SID, por até 3 meses), vitamina E (400 UI/20 kg de peso vivo, VO, SID) e ômega 3 (1 g/kg, VO, SID).2 A ressecção cirúrgica é recomendada, tendo demonstrado um bom controle a longo prazo em cães e gatos.3 Também são citadas a quimioterapia intralesional (cisplatina ou carboplatina, 1,5 mg/cm³, a cada 7 dias, até remissão), fototerapia, a criocirurgia e a eletroquimioterapia como ferramentas de controle.2 O uso de eletroquimioterapia (EQT) com bleomicina intralesional (1 UI/cm³ de tumor) ou intravenosa (15000 UI/m²) tem se mostrado muito efetiva em gatos, principalmente em casos em que a ressecção cirúrgica se torna desafiadora.3
A quimioterapia sistêmica também é citada, com uso de carboplatina (250 a 300 mg/m², a cada 21 dias, de 4 a 6 sessões) ou a doxorrubicina (30 mg/m² a cada 21 dias, de 4 a 6 sessões), mas seus resultados não oferecem uma regressão satisfatória.2 A Terapia Fotodinâmica (TFD) é amplamente utilizada no tratamento de CCE em felinos, principalmente com ftalocianina de cloro-alumínio, se mostrando eficaz no tratamento de lesões superficiais.3
A EQT é um procedimento quimioterápico potencializado pela eletroporação da membrana citoplasmática por meio de pulsos elétricos, e essa técnica permite que ocorra uma penetração mais eficaz e localizada de fármacos quimioterápicos no citoplasma de células.2 Ela se baseia em aumentar a permeabilidade da membrana das células tumorais, fazendo com que quimioterápicos não tão potentes consigam adentrar essas células através dos pulsos elétricos feitos nos locais com tumoração (Figura 1).9,10
Figura 1 – Mecanismos de perfusão da bleomicina após eletroporação.
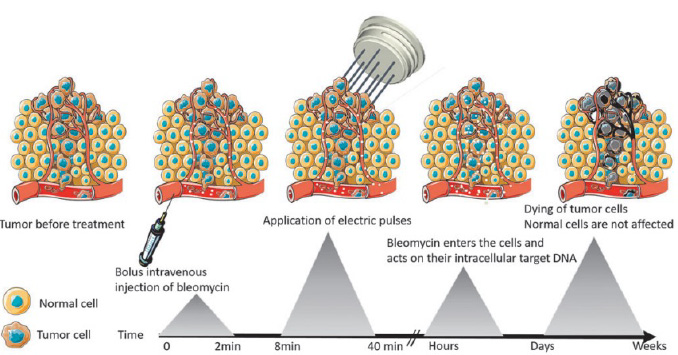
A eletroporação pode ser dividida em quatro fases: indução, onde o campo elétrico induz a alteração no potencial de membrana e tende a provocar defeitos quando atinge cerca de 200 mV.2 Expansão, ocorre a ampliação do defeito por tempo proporcional à presença do campo elétrico. Estabilização, a redução do campo elétrico leva a uma estagnação do processo, e a membrana se torna permeável a pequenas moléculas. E por fim o selamento, onde a membrana volta a ser selada em um processo lento.
Casos em que a bleomicina na EQT não surtem o efeito desejado podem ter a substituição do fármaco por gencitabina.9 Outro uso é a cisplatina e seus análogos, que agem se ligando às bases de DNA, levando à ligação cruzada de DNA, causando a morte celular. Seu uso associado à EQT é potencializado, mas não é recomendado em gatos devido à sua alta toxicidade nessa espécie.11 Uma alternativa relatada é o uso do cálcio, que também possui grande potencial de necrose tumoral, além de ser uma alternativa mais barata e que traz um nível maior de biossegurança quando comparada aos antineoplásicos, mas pode acarretar maior chance de reação inflamatória local.9 A doxorrubicina e a mitoxantrona são quimioterápicos com ações similares que também potencializados com a EQT.11
MATERIAIS E MÉTODOS
A pesquisa desse trabalho segue um modelo de análise descritivo, que utiliza de um estudo de caso para a sua elaboração, com abordagem qualitativa. O atendimento do paciente foi feito na Clínica Veterinária Baschirotto, localizada em Criciúma/SC.
Os materiais consultados incluem o prontuário do paciente, com histórico médico e dados do exame clínico, bem como exames, imagens e informações sobre o procedimento cirúrgico. Para analisar a relevância deste estudo, foi utilizado um comparativo dos sinais clínicos apresentados pelo paciente antes e depois do procedimento, bem como se houve resolução do quadro em um aspecto geral. O pós-operatório do paciente foi descrito para averiguar se houve alguma complicação ou não. Por fim, para definir se essa técnica empregada foi bem-sucedida, a presente literatura consultada, sendo principalmente as obras de Kudnig e Séguin (2022), Impellizeri (2021), Vail, Thamm e Liptak (2020), Daleck e de Nardi (2017) e Meuten (2017), auxiliou em um comparativo com o resultado do tratamento proposto ao paciente.1,2,3,6,9
RELATO DE CASO
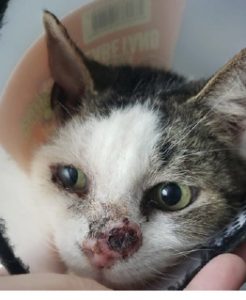
No dia 21/06/2021 foi atendido na Clínica Veterinária Baschirotto, localizada em Criciúma/SC, um felino, macho, sem raça definida (SRD), castrado, pelagem branca e cinza, 16 anos de idade, pesando 4kg com histórico de lesão ulcerada e crostosa em plano nasal (Figura 2) presente desde janeiro de 2021, já diagnosticado anteriormente como FeLV positivo.
Foi relatado pela tutora que o felino tinha livre acesso à rua e ficava rotineiramente exposto ao sol. Ao exame físico apresentou parâmetros fisiológicos como temperatura retal, frequência cardíaca e respiratória e tempo de perfusão capilar dentro dos valores de referência. Os sinais clínicos observados foram lesão ulcerada e crostosa em plano nasal, medindo 2 cm x 3 cm e distrição respiratória, não apresentando linfadenomegalia.
O animal não apresentou alterações hematológicas e bioquímicas importantes. O diagnóstico foi presuntivo baseado na apresentação clínica da lesão, que estava presente somente em áreas despigmentadas, bem como histórico de exposição solar excessiva. Com a caracterização do quadro, em dezembro de 2021 foi decidido que o paciente seria submetido ao procedimento de EQT associada à bleomicina, preconizando realizar uma só sessão.
A medicação pré-anestésica utilizada foi metadona, dose de 0,3 mg/kg (IM) e acepromazina 0,07 mg/kg (IM). Anestesia local foi preconizada utilizando lidocaína sem vasoconstritor, na dose de 2 mg/kg, em cada lateral da face, fazendo o bloqueio do nervo maxilar pelo forame maxilar. Cetamina e propofol foram escolhidos para indução, na dose de 0,6 mg/kg (IV) e 3 mg/kg (IV) respectivamente. A manutenção anestésica foi obtida por inalação de isoflurano diluído em oxigênio 100%, mantido ao efeito, em sistema circular valvular (com reinalação) e resgates em bolus de fentanil na dose de 4 µg/kg no transoperatório. O paciente foi mantido em decúbito esternal, com o pescoço em ventroflexão, e a região de plano nasal foi devidamente antissepsiada com clorexidine 2% e álcool 70%.
A dosagem de bleomicina foi determinada conforme a área de superfície corporal, calculada utilizando a dose de 15000 UI/m². Após 7 minutos da aplicação de bleomicina, a eletroporação do tumor foi realizada com o pulso elétrico gerador usando eletrodos de 6 agulhas de aço inoxidável paralelos (Figura 3). Foram entregues oito pulsos elétricos com amplitude de 750 V/cm, realizando varredura em toda a extensão tumoral e margens.

No pós-cirúrgico foram administrados convenia, via SC, única aplicação, na dose de 8 mg/kg e robenacoxibe, VO, SID, durante 5 dias na dose de 2 mg/kg, além de recomendação do uso de Oxcell 500, 1 comprimido ao dia. Foi orientado ao tutor que fosse feita a limpeza da região com solução fisiológica 0,9% e spray de clorexidine 1%, duas vezes ao dia, durante 7 dias. Durante os primeiros dias de pós-operatório foi possível observar uma leve inflamação na lesão tratada.
Após 25 dias, as crostas ali presentes foram se desprendendo e um tecido cicatricial foi se formando.
A regressão total se deu após 35 dias, sendo possível observar a sua evolução pós-operatória na Figura 4.
Figura 4 – Evolução do quadro clínico do paciente
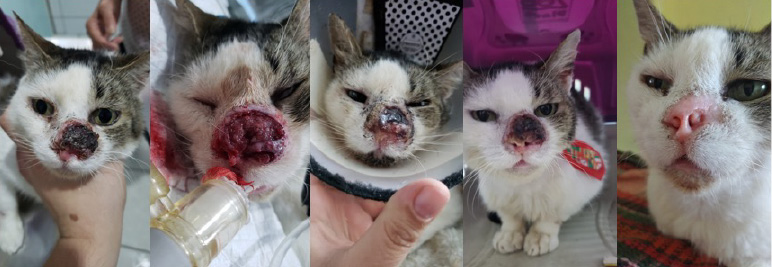
RESULTADOS E DISCUSSÃO
O CCE é uma neoplasia formada a partir das células da epiderme, uma neoformação maligna dos queratinócitos, podendo ocorrer com crescimento lento e não necessariamente metastático. Felinos são os mais acometidos, no entanto há relatos em bovinos, caninos e eqüinos.12-14
Nos gatos, o carcinoma espinocelular encontra-se intimamente relacionado a exposição solar, com uma distribuição clássica de lesões localizadas na face, e nas áreas com pouco pelo: plano nasal, pinas e pálpebras,15 o que corrobora com o que é afirmado por Daleck e de Nardi (2016) e Meuten (2016).1,2 O paciente do caso relatado possuía região de plano nasal despigmentada, onde encontrava-se a lesão, em locais também comuns de apresentação do CEC como ponta de orelha, o paciente possuía pelagem escura o qual não apresentava lesão relacionadas a enfermidade, além de contato excessivo ao sol.
Quanto a predisposição, o CCE ocorre em cães idosos, de ambos os sexos, com maior incidência entre 6 e 10 anos. As raças Keeshond, Schnauzer, Basset Hound, Collie, Dálmata, Pitbull Terrier e Beagle estão sob maior risco. Cães de pelo curto e manto piloso ventral branco ou malhado também estão predispostos. Em gatos, não há predisposição sexual ou racial, contudo, observa-se maior incidência em pacientes entre 9 e 14 anos de idade, aqueles com pelos faciais brancos ou pelagem branca.15
Os primeiros relatos do efeito antitumoral associado ao uso de corrente elétrica foram realizados do final do século 18, com o uso de corrente contínua de baixa intensidade, estudos mais elaborados sobre as possíveis aplicações terapêuticas e os mecanismos envolvidos foram realizados para o final do século 20, resultando nas duas principais terapias elétricas contra o câncer mais bem estudadas: eletroquimioterapia e eletroterapia. Diversos estudos clínicos em países como França, Eslovênia, Dinamarca, Irlanda, Itália, EUA, Japão, México, Áustria e Austrália já foram realizados com a eletroquimioterapia.16
O uso de EQT tratando CCE foi reportado pela primeira vez em 2003, onde foi utilizada a bleomicina como fármaco quimioterápico, tendo resultado satisfatório na maioria dos casos.9 Tozon et al. (2014) posteriormente confirmou a eficácia dessa associação, tratando 11 gatos com a neoplasia, sendo que 87,5% dos casos tiveram regressão.17 Spugnini et al. (2015) comparou a eficácia da bleomicina via IV com e sem eletroporação.18 Os resultados mostraram que a bleomicina associada à EQT traz um resultado melhor e a longo prazo, com efeito citotóxico potencializado.
O exato mecanismo pelo qual o dano ao DNA dispara o gatilho para a morte celular ainda não é perfeitamente conhecido, no entanto, o mecanismo de ação da bleomicina consiste na fragmentação do DNA, o que gera a interrupção da fase G2-M do ciclo da célula neoplásica, e é extremamente potencializado com o uso da EQT, sendo que esta mimetiza os efeitos da radioterapia por produzir dano na fita simples e na dupla, na via catalítica.2,11 A necrose parcial tumoral logo após o seu uso não necessita de abordagens cicatriciais de feridas e causa pouquíssimas reações inflamatórias do tecido circundante; na primeira semana é esperada uma ulceração com reação inflamatória leve circundante, seguida por uma formação crostosa superficial, que desaparece em 5 semanas.9 O paciente do caso relatado teve uma melhora significativa após 35 dias, o que indica uma recuperação rápida e sem complicações.
Uma grande vantagem é que os efeitos citotóxicos adversos são minimizados, já que a alta citotoxicidade de drogas polartóxicas (como a bleomicina ou a cisplatina) pode ser obtida mesmo que sua concentração externa seja baixa, pois somente o local etroporado é afetado. Essa permeabilização temporária permite o livre trânsito de moléculas, íons e água entre os dois lados da membrana celular.11 Além disso, apresenta vantagens como o pequeno número de aplicações, baixo custo e alta efetividade.2 O procedimento de EQT realizado neste estudo foi em uma única aplicação, sem causar danos citotóxicos em tecidos saudáveis, corroborando com os autores citados.
Pacientes que apresentam carcinoma de células escamosas, em sua maioria, apresentam uma condição avançada da doença ao serem diagnosticados, por esse motivo a excisão cirúrgica torna-se mais difícil.18 Sendo assim, a eletroquimioterapia é uma alternativa terapêutica que demonstra importante taxa de controle e preservação de estruturas anatômicas dos pacientes.
Após analisar as possibilidades de tratamento para o CCE bem como os relatos descritos em literatura, pode-se observar que a eletroquimioterapia é considerada uma opção pouco invasiva comparada a excisão cirúrgica e que demonstra significativa taxa de cura para O CCE em felinos, fato este que foi observado no paciente do caso relatado.
CONCLUSÃO
É evidente o aumento do número de felinos como animais de companhia. O carcinoma de células escamosas está entre os tumores de maior incidência nessa espécie, principalmente nos animais com a pele e pelagem claras. Dentre as terapêuticas propostas pela literatura, a eletroquimioterapia associada à bleomicina se mostra eficaz no tratamento desta patologia, dando melhor qualidade de vida e remissão das células tumorais de forma pouco invasiva e agressiva, exibindo resultados satisfatórios na tentativa de controle do CCE.
Procedimentos cirúrgicos de remoção de massas requerem uma ampla margem para alcançar a maior probabilidade de cura possível, mas muitas vezes podem não garantir completa funcionabilidade da região acometida, bem como ter complicações pós-cirúrgicas. A presente literatura não traz relatos parecidos quanto ao uso de EQT associada ou não à cirurgia, o que torna essa modalidade terapêutica extremamente interessante para a Medicina Veterinária.
Dentre as vantagens da eletroquimioterapia, destaca-se a rapidez e praticidade na execução do protocolo eletroquimioterápico e inexistência de complicações trans/pós-terapêuticas. Desta forma, pode-se concluir que a EQT é uma das melhores opções para o tratamento do carcinoma de células escamosas especialmente na forma cutânea da doença em felinos.
AGRADECIMENTOS
As autoras agradecem à Clínica Veterinária Baschirotto e a sua respectiva equipe de colaboradores por disponibilizarem as informações necessárias para a construção desse artigo, bem como por todo o cuidado com o paciente.
DECLARAÇÃO DE CONFLITO DE INTERESSE
As autoras declaram que não possuem conflito de interesse.
CONTRIBUIÇÕES DAS AUTORAS
Todas as autoras contribuíram para o desenvolvimento desse manuscrito. A revisão e os ajustes foram repassados e confirmados pelos autores até a chegada da versão final deste documento.
REFERÊNCIAS
1.MEUTEN, Donald J. Tumors in Domestic Animals. John Wiley & Sons, 5 ed. 2017.
2.DALECK, Carlos Roberto; DE NARDI, Rodrigo Barboza. Oncologia em Cães e Gatos. Roca, 2 ed. Rio de Janeiro, 2016.
3.VAIL, David M.; THAMM, Douglas H.; LIPTAK, Julius M. Withrow & McEwen’s Small Animal Clinical Oncology. Elsevier, 6 ed., 2020.
4.PÉREZ-ENRIQUEZ, Juan Miguel; ROMERO-ROMERO, Laura; ALONSO-MORALES, Rogelio Alejandro; FUENTES-PANANÁ, Ezequiel M. Tumor prevalence in cats: experience from a reference diagnostic center in mexico city (2006-2018). Veterinaria México Oa, Mexico City, v. 7, n. 4, p. 1-14, 11 dez. 2020. Universidad Nacional Autonoma de Mexico.
5.ETTINGER, Steve; FELDMAN, Edward; CÔTE, Etienne. Textbook of Veterinary Internal Medicine: Diseases of the Dog and the Cat. Elsevier, 8 ed. St. Louis, 2017.
6.KUDNIG, Simon T.; SÉGUIN, Bernard. Veterinary Surgery Oncology. John Wiley & Sons, 2 ed., 2022.
7.CRIVElLLENTI, Leandro Z.; BORIN-CRIVELLENTI. Casos De Rotina Em Medicina Veterinária De Pequenos Animais. Medvet: Sao Paulo. 1ed. 840p. 2015
8.SPUGNINI, E. P.; AZZARITO, T.; FAIS, S.; FANCIULLI, M.; BALDI, A. Electrochemotherapy as First Line Cancer Treatment: Experiences from Veterinary Medicine in Developing Novel Protocols. Current Cancer Drug Targets, v. 16, n.1, p. 43–52, 2016. doi:10.2174/156800961601151218155
9.IMPELLIZERI, Joseph A. Electroporation in Veterinary Oncology Practice. Springer, 1 ed., New York, 2021.
10.CEMAZAR, M., & SERSA, G. Recent Advances in Electrochemotherapy. Bioelectricity, v. 1, n. 4, 2019. doi:10.1089/bioe.2019.0028
11.SPUGNINI, E. P.; BALDI, A. Electrochemotherapy in Veterinary Oncology. Veterinary Clinics of North America: Small Animal Practice. Caserta, v. 47, n. 19., 2019. doi:10.1016/j.cvsm.2019.04.006
12.GOLDSCHIMIDT, M. H. et al. Tumors of the skin and soft tissues. In: MEUTEN, D. J. Tumors in domestic animals. 4. ed. Iowa: Iowa State Press, cap. 2, p. 45-117, 2002.
13.SOUZA, T. M. Estudo retrospectivo de 761 tumores cutâneos em cães. 2005. 296f. Dissertação (Mestrado em Concentração em Patologia Veterinária) – Universidade Federal de Santa Maria, Santa Maria, 2005.
14.SCOPEL, D. et al. Estudo Retrospectivo da Casuística de Carcinoma de Células Escamosas em Felinos, Bovinos, Caninos, Equinos e Ovinos entre os Anos de 2002 e 2006 no Laboratório Regional de Diagnósticos (LRD) /UFPEL. In: CIC (Congresso de Iniciação Científica de Pesquisa e Responsabilidade Ambiental) 16, Pelotas. Anais co XVI CIC. Pelotas: UFPEL, p.4, 2007.
15.HORTA, Rodrigo dos Santos; CAMPOS, Cecilia Bonolo de; LAVALLE, Gleidice Eunice. Biologia Tumoral. In: HORTA, Rodrigo dos Santos. Oncologia em Pequenos animais. Minas Gerais: FEP MVZ Editora. 2013. Cap. 2. P. 11-28
16.JERICÓ, Márcia Marques; ANDRADE NETO, João Pedro de; KOGIKA, Márcia Mery. Tratado de medicina interna de cães e gatos. São Paulo: Roca, 1 ed. 2015.
17.TOZON, N.; PAVLIN, D.; SERŠA, G. et al Electrochemotherapy with intravenous bleomycin injection: an observational study in superficial squamous cell carcinoma in cats. J Feline Med Surg v. 16, p. 291–299, 2014. https://doi.org/10.1177/1098612X13507071
18.SPUGNINI E. P.; PIZZUTO, M.; FILIPPONI, M. et al. Electroporation Enhances Bleomycin Efficacy in Cats with Periocular Carcinoma and Advanced Squamous Cell Carcinoma of the Head. J Vet Intern Med. v.29, p.1368–75, 2015.

Luana Probst
Graduada no Centro Universitário Barriga Verde – UNIBAVE (2018). Pós-graduada em oncologia clínica e cirurgia pelo Instituto Qualittas (2020). Profissional capacitada em eletroquimioterapia pelo Centro de Oncologia Vetcâncer (2019) e em criocirurgia pelo Instituto Qualittas (2019). Aperfeiçoamento em cirurgia oncológica e reconstrutiva pela Unesp (2022).

Letícia Cardoso
Médica Veterinária formada pelo Centro Universitário Barriga Verde – UNIBAVE (2022).

Morgana de Souza
Graduanda de Medicina Veterinária pela Universidade do Sul de Santa Catarina – UNISUL (2022).
{PAYWALL_FIM}