Por M.V. Matheus Daudt
Achados ultrassonográficos abdominais em cães endocrinopatas
As endocrinopatias são cada vez mais frequentes na rotina clínica de cães e gatos e compreendem cerca de 10% da casuística dos atendimentos, onde o hiperadrenocorticismo e diabetes mellitus são mais comumente observados. Diante desse panorama, o presente trabalho, visa abordar os principais achados de imagem ultrassonográfica em cães endocrinopatas.
{PAYWALL_INICIO}
1 – Glândulas adrenais:
O hiperadrenocorticismo (HAC) é caracterizado pela concentração sanguínea de cortisol elevada, podendo ser secundário a administração crônica de glicocorticoides (HAC iatrogênico) ou pela produção excessiva das glândulas adrenais (HAC endógeno). O HAC endógeno pode ser classificado em: HAC ACTH dependente (hipófise-dependente), devido a um tumor hipofisário ou HAC ACTH independente, resultante de tumores funcionais do córtex adrenal. Nos pacientes com HAC iatrogênico geralmente observa-se na ultrassonografia a atrofia glandular bilateral, diferentemente dos pacientes HAC ACTH dependente, onde ambas as adrenais se apresentam hiperplásicas pela resposta hormonal. Em pacientes diagnosticados com HAC ACTH independente, pode-se observar formação ou nódulo em adrenal, podendo estar aumentada, além de possíveis alterações de seu formato anatômico ou contornos abaulados (figura 1), nestes pacientes normalmente ocorre atrofia da glândula contralateral (DE MARCO, 2017).
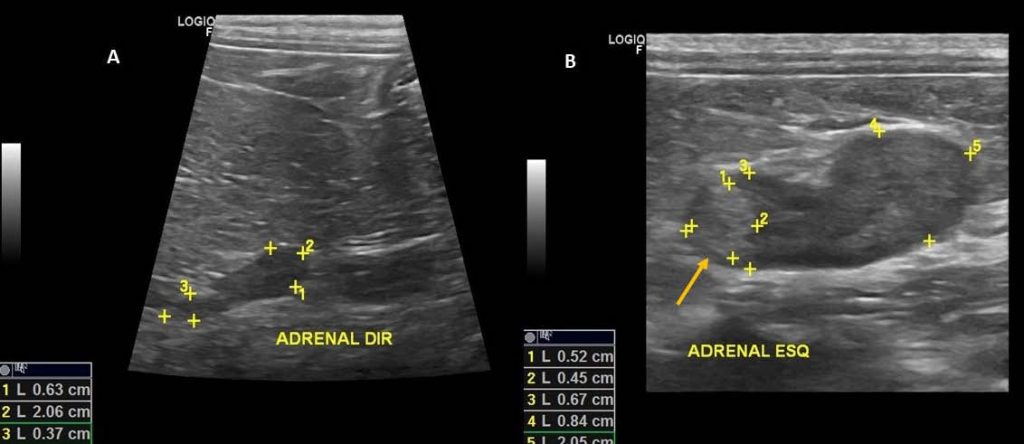
Diversas são as razões para a avaliação ultrassonográfica de cães com suspeita de HAC, como, por exemplo, descartar doenças não adrenais e corroborar com a suspeita clínica principalmente no achado de adrenomegalia, bem como outros achados em órgãos abdominais, pois a mesma pode ajudar a distinguir entre os diferentes tipos de hiperadrenocorticismo, sendo importante detectar a atrofia da glândula adrenal contralateral para auxílio no diagnóstico de hiperadrenocorticismo ACTH independente em casos de assimetria de adrenal, onde há um aumento expressivo de uma adrenal por nódulo ou formação (BENCHEKROUN et. al, 2010).
Muitos estudos foram feitos a fim de padronizar valores de referência das glândulas adrenais em cães saudáveis (espessura, comprimento e largura), porém, estudos mais recentes, estabeleceram intervalos de referência para espessura dos polos em plano sagital (pois este plano possui menor variação interobservador) em diferentes categorias de peso, devido a comprovada relação entre as dimensões ultrassonográficas das glândulas adrenais com o peso corporal de cães saudáveis. (SOULSBY et al, 2014; MELIÁN et. al, 2021; BENTO et. al., 2016).
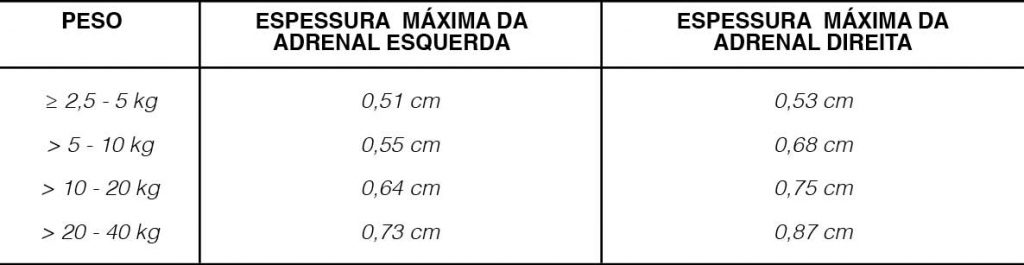
Soulsby et. al (2014) avaliaram as dimensões das glândulas adrenais de 45 cães saudáveis em três categorias de peso (<10 kg, 10-30 e >30 kg), porém com um número amostral pequeno (15 animais em cada grupo) (quadro 1). Outro estudo conduzido por Bento et, al. (2016) mensurou a espessura do polo caudal das adrenais de 266 cães sem doença adrenal, para determinar se há relação entre a espessura da adrenal com sexo, idade e peso dos animais, onde concluíram que a idade e sexo estavam significativamente associados com a espessura das glândulas, sendo maior em machos que em fêmeas, e a espessura da adrenal esquerda aumentou com a idade, ressaltando a importância de se levar em consideração essas variáveis ao avaliar as glândulas de cães sem doença adrenal e observaram que a espessura das adrenais em cães com peso ≤12 kg foi menor que em cães com peso >12 kg nesse estudo (quadro 2). Melián et. al (2021), com intuito de propor intervalos de referência mais precisos para a espessura das glândulas adrenais em cães saudáveis, dividiu os animais em quatro categorias de peso (≥ 2,5 – 5 kg, > 5 -10 kg, >10 – 20 kg e > 20- 40 kg) onde a sensibilidade para detectar adrenomegalia em cães com HAC foi de 95,6%. (quadro 3).


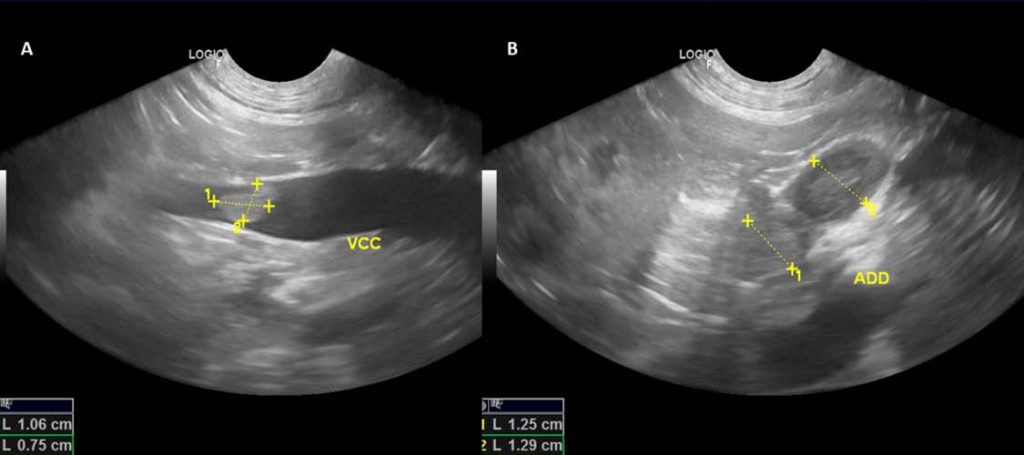
Tumores adrenocorticais são relativamente comuns em cães e correspondem de 10- 20% da ocorrência de HAC. Os feocromocitomas são descritos como mais propensos a invadirem vasos adjacentes e o exame ultrassonográfico se mostrou 100% sensível e 96% específico na identificação de trombo neoplásico na região da veia cava caudal. (figura 2) (DAVIS, SCHOCHET, WRIGLEY; 2012).
2 – Fígado e Vesícula biliar:
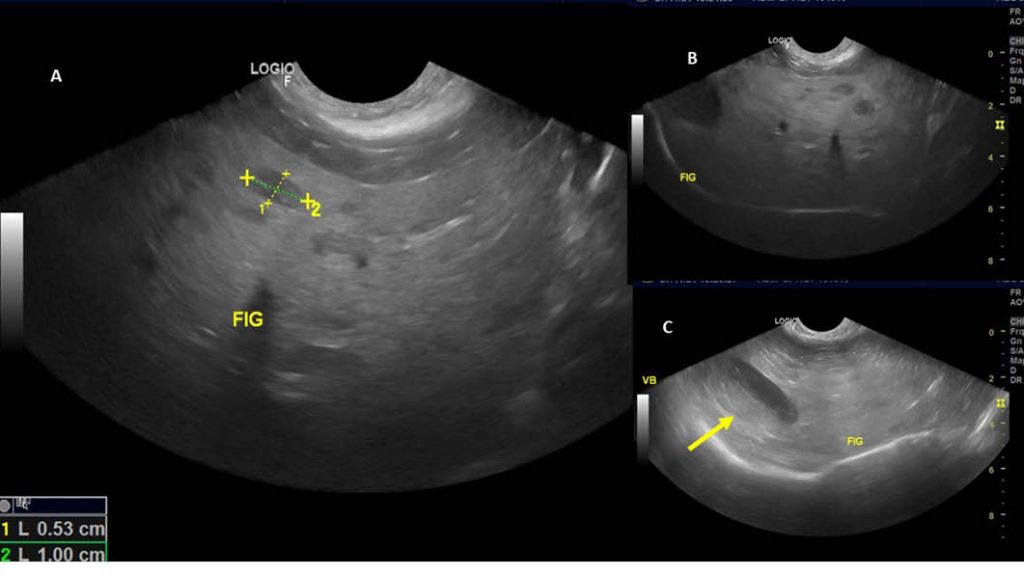
A hepatopatia vacuolar esteroidal se caracteriza pelo aumento difuso da ecogenicidade hepática, podendo causar atenuação do feixe sonoro e, também, podem ser detectadas lesões focais hipoecogênicas secundárias ao dano tecidual (hiperplasias nodulares benignas) (Figura 3). Em 75 a 90% dos casos é possível observar hepatomegalia e parece haver uma associação entre a hepatopatia vacuolar grave e a mucocele biliar. (SEPESY et al., 2006; GUILLOT et al., 2009).
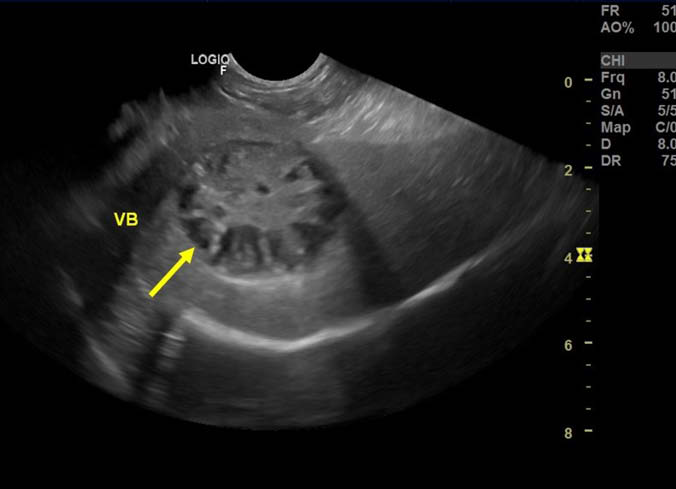
A relação da ocorrência de mucocele biliar em pacientes com diabetes mellitus e HAC já tem sido frequentemente descrita, onde, a chance de desenvolver mucocele biliar é 29 vezes maior em cães com HAC do que em cães sem endocrinopatias. Sua etiologia é indeterminada e multifatorial, ocorre pelo acúmulo de bile em decorrência da estase biliar e hiperlipidemia levando a hiperplasia mucinosa, tornando a bile gelatinosa, imóvel e organizada, dando um padrão estrelado/estriado (figura 4) podendo levar a ruptura da vesícula biliar. (MEISCH et al., 2009; BESSO et. al., 2000).
3 – Pâncreas:
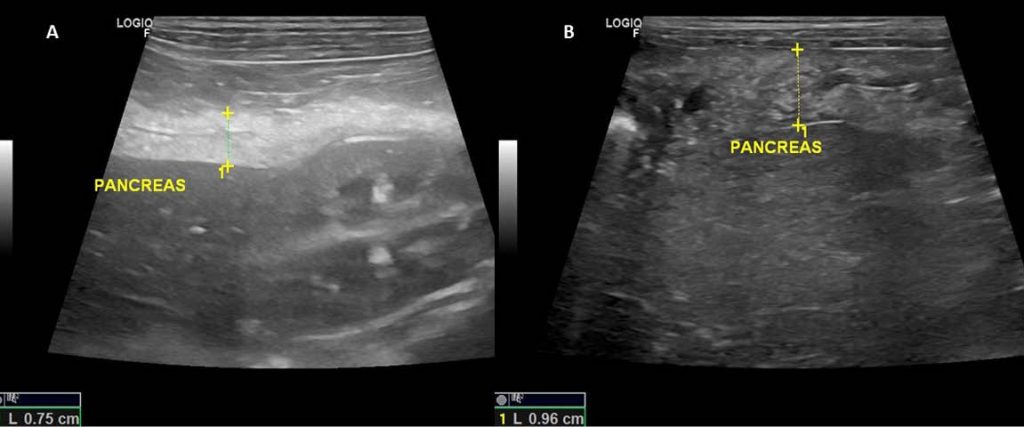
Em relação ao pâncreas, o achado ultrassonográfico mais frequente nas endocrinopatias é aumento da ecogenicidade (figura 5). A hiperecogenicidade pancreática já foi descrita como estatisticamente maior em cães com hiperadrenocorticismo quando comparado com a ecogenicidade do pâncreas em cães saudáveis, não tendo a idade, o sexo e o escore corporal uma influência direta neste achado em cães saudáveis (GRANGER et. al; 2015). A concentração sérica da lipase pancreática canina específica se mostrou aumentada em cães com HAC e pode estar relacionada a dislipidemia subjacente, o que pode sugerir que esses cães apresentam um risco aumentado de inflamação pancreática subclínica. (MAWBY, WHITTEMORE, FECTEAU; 2014). Brostrom et. al. (2013), em um estudo com 61 cães, mostrou que a pancreatite crônica é mais frequentemente encontrada em cães com endocrinopatias do que em cães saudáveis, sendo que, a maioria dos cães do estudo, apresentava diabetes mellitus. A mineralização é uma causa potencial de aumento da ecogenicidade pancreática em cães com hiperadrenocorticismo e a deposição gordurosa tem sido associada como a principal causa de aumento da ecogenicidade pancreática em humanos, após a administração oral contínua de corticosteroides por seis meses (GUPTA, ARENSON, MCKEE; 1987).
4 – Vesícula urinária:
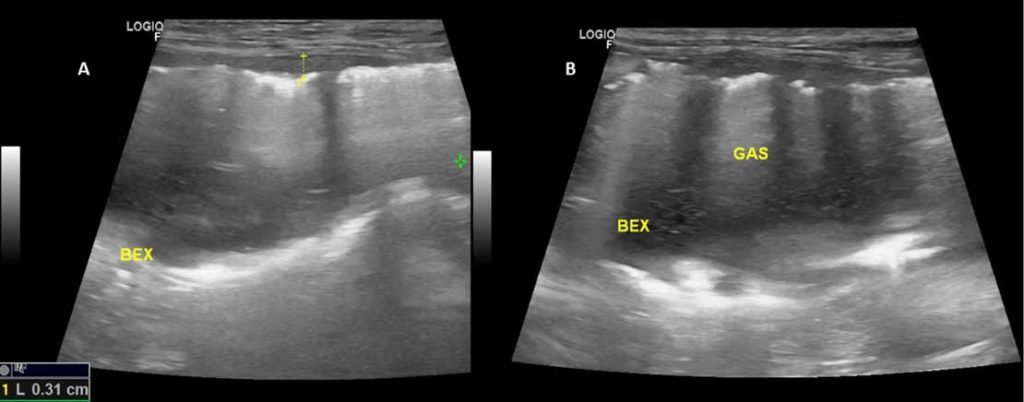
A cistite enfisematosa é uma infecção complicada e incomum da vesícula urinária pela presença de microrganismos fermentadores de glicose (bactérias ou leveduras), tem sido relacionada com diabetes mellitus em cães e gatos, devido a glicosúria e a baixa imunidade desses pacientes, tornando-se fatores predisponentes, porém, sua ocorrência já foi relatada em cães não diabéticos. A cistite enfisematosa é identificada na ultrassonografia pela visibilização de artefatos de reverberação intramural e intraluminal, que caracteriza a presença de gás (figura 6). (MOON, BILLER, SMEE; 2014)
5 – Calcificações distróficas:
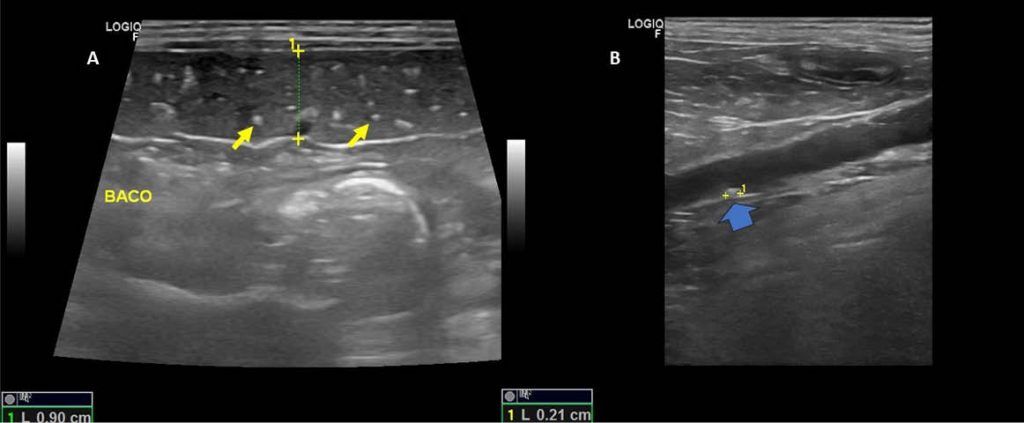
Podemos observar, em alguns casos de cães com hiperadrenocorticismo, a deposição de cálcio em tecidos, como músculo esquelético, fígado, anéis traqueais e, frequentemente, em baço (figura 7). Sua patogênese ainda é desconhecida e geralmente as concentrações de cálcio plasmático estão normais nesses pacientes. Acredita-se que possa estar relacionada com o rearranjo da estrutura molecular das proteínas (elastina e colágeno) e na formação de uma matriz orgânica que atrai e liga o cálcio. (MELIÁN, PÉREZ-ALENZA; 2017; HERRTAGE, 2011)
Conforme demonstrado, a ultrassonografia abdominal é uma ferramenta indispensável no auxílio diagnóstico de pacientes com suspeita de endocrinopatias assim como para avaliar o grau de repercussão dessas doenças nos demais órgãos, podendo fornecer informações valiosas e que corroboram com a suspeita clínica.
REFERÊNCIAS:
BENCHEKROUN, G.; DE FORNEL-THIBAUD, P.; RODRÍGUEZ PIÑEIRO, M.I.; RAULT, D.; BESSO, J.; CHOEN, A.; HERNANDEZ, J.; STAMBOULI, F.; GOMES, E.; GARNIER, F.; BEGON, D.; MAUREY-GUENEC, C.; ROSENBERG, D. Ultrasonography Criteria for Differentiating ACTH Dependency from ACTH Independency in 47 Dogs with Hyperadrenocorticism and Equivocal Adrenal Asymmetry. J Vet Intern Med, v.24, p.1077-1085, 2010.
BENTO, P.L.; CENTER, S.A.; RANDOLPH, J.F.; YEAGER, A.E.; BICALHO, R.C. Associations between sex, body weight, age, and ultrasonographically determined adrenal gland thickness in dogs with non–adrenal gland illness. JAVMA, v.248, No.6, p.652-660, 2016.
BESSO, J.G.; WRIGLEY, R.H.; GLIATTO, J.M.; WEBSTER, C.R.L. Ultrasonographic appearance and clinical findings in 14 dogs with gallbladder mucocele. Veterinary Radiology & Ultrasound, v.41, No.3, p.261-271, 2000.
BOSTROM, B.M.; XENOULIS, P.G.; NEWMAN, S.J.; POOL, R.R.; FOSGATE, G.T.; STEINER, J.M. Chronic pancreatitis in dogs: A retrospective study of clinical, clinicopathological, and histopathological findings in 61 cases. The Veterinary Journal, v.195, p.73-79, 2013.
DAVIS, M.K.; SCHOCHET, R.A.; WRIGLEY, R. Ultrasonographic identification of vascular invasion by adrenal tumors in dogs. Veterinary Radiology & Ultrasound, v.00, No.0, p.1-4, 2012.
DE MARCO, V. Hiperadrenocorticismo canino. In: Tratado de medicina interna de cães e gatos. Rocca, Rio de Janeiro, 1 ed, p.1691-1703, 2017.
GRANGER, L.A; HILFERTY, M.; FRANCIS, T., STEINER, J.M, GASCHEN, L. Variability in the ultrasonographic appearance of the pancreas in healthy dogs compared to dogs with hyperadrenocorticism. Vet Radiol Ultrasound. v.00, No.0, p.1-9, 2015.
GUILLOT, M.; D’ANJOU, M.A.; ALEXANDER, K.; BÉDARD, C.; DESNOYERS, M.; BEAUREGARD, G.; DEL CASTILLO, J.R.E. Can sonographic findings predict the results of liver aspirates in dogs with suspected liver disease?. Veterinary Radiology & Ultrasound, v.50, No.5, p.513-518, 2009.
GUPTA, A.K.; ARENSON, A.M.; MCKEE, J.D. Effect of steroid ingestion on pancreatic echogenicity. J Clin Ultrasound. v.15 p.171–174, 1987.
HERRTAGE, M.E. Diagnosing canine hyperadrenocorticism. In: World Small Animal Veterinary Association World Congress Proceedings. Jeju, Korea, 2011.
MAWBY, D.I.; WHITTEMORE, J.C.; FECTEAU, K.A. Canine pancreatic-specific lipase concentrations in clinically healthy dogs and dogs with naturally occurring hyperadrenocorticism. J Vet Intern Med, v.28, p.1244-1250, 2014.
MELIÁN C.; PÉREZ-ALENZA, D.; hyperadrenocorticism in dogs. In: Textbook of veterinary internal medicine: diseases of the dog and the cat. Elsevier, St. Louis, Missouri, 8 ed., v.02, p.4345-4389, 2017.
MELIÁN C., PÉREZ-LÓPEZ L., SAAVEDRA P., RAVELO-GARCÍA AG., SANTOS Y., JABER JR. Ultrasound evaluation of adrenal gland size in clinically healthy dogs and in dogs with hyperadrenocorticism. Vet Rec, e.80, 2021.
MESICH, M.L.L.; MAYHEW, P.D.; PAEK, M.; HOLT, D.E; BROWN, D.C. Gall bladder mucoceles and their association with endocrinopathies in dogs: a retrospective case-control study. Journal of Small Animal Practice, v.50, p.630-635, 2009.
MOON, R.; BILLER, D.S.; SMEE, N.M. Emphysematous cystitis and pyelonephritis in a nondiabetic dog and a diabetic cat. J Am Anim Hosp Assoc, v.50, p.124-129, 2014.
SEPESY L.M.; CENTER S.A.; RANDOLPH J.F; WARNER K.L; ERB H.N. Vacuolar hepatopathy in dogs: 336 cases (1993–2005). J Am Vet Med Assoc, v.229, p.246-252, 2006.
SOULSBY, S.N.; HOLLAND, M.; HUDSON, J.A.; BEHREND, E.N. Ultrasonographic evaluation of adrenal gland size compared to body weight in normal dogs. Vet Radiol Ultrasound, v.00, No.0, p.1-10, 2014.
WANG, K.Y.; PANCIERA, D.L.; AL-RUKIBAT, R.K.; RADI, Z.A. Accuracy of ultrasound-guided fine-needle aspiration of the liver and cytologic findings in dogs and cats: 97 cases (1990–2000). J Am Vet Med Assoc, v.224, p.75-78, 2004.

M.V. Matheus Daudt
Professor auxiliar I de Fundamentos em radiologia e ultrassonografia veterinária do curso de medicina veterinária da universidade Estácio de Sá (UNESA-RJ). Ministra aulas em cursos de capacitação e educação continuada no Centro de ensino em ultrassonografia veterinária (CENUS-Solvet). Médico veterinário ultrassonografista do H&Diagnóstico (Centro de diagnóstico localizado no Rio de Janeiro). Foi médico veterinário do setor de ultrassonografia da Policlínica escola de Medicina veterinária da universidade Estácio de Sá de 2017 a 2021.
{PAYWALL_FIM}
